RESPONSABILI DELLA RICERCA
Team di ricerca
U. Bracale, E. De Benedetto, R. Peltrini
Partenariati e/o collaborazioni in essere (se esistenti)
Campus Biomedico di Roma
Tipo di attività prevalente
Accademica con ricadute applicative
Ricadute applicative
Chirurgia
Descrizione dell'attività di ricerca
L’attività di ricerca è basata sull’impiego di algoritmo innovativi, basati su tecniche di Intelligenza Artificiale allo scopo di valutare automaticamente la qualità della vascolarizzazione del settore intestinale dopo resezione nell’ambito della chirurgia laparoscopica colo-rettale. Un flusso sanguigno residuo ottimale è auspicabile al fine di prevenire complicazioni legate al ripristino della continuità digesiva (anastomosi intestinale). Allo stato attuale, infatti, tale valutazione viene compiuta esclusivamente in maniera soggettiva dai chirurghi, i quali hanno tra i più moderni ed utili mezzi di supporto il cosiddetto “verde indocianina”.
Il verde indocianina (in abbreviato ICG) è una molecola sviluppata negli anni ‘50 inizialmente per essere applicata alla fotografia ad infrarossi, poiché la principale peculiarità di questa sostanza è che diventa fluorescente se illuminata con una luce ad infrarossi. La somministrazione al paziente di tale sostanza è endovenosa o peritumorale ed avviene tipicamente il giorno prima dell’intervento o in fase intraoperatoria. Conseguentemente, la molecola si lega alle proteine plasmatiche presenti nel sangue, emettendo la sua fluorescenza a livello del circolo sanguigno, epatico e biliare quando viene in contatto con luce a infrarosso. Dunque, nell’ambito della chirurgia laparoscopica, la qualità della vascolarizzazione viene valutata sulla base della luminosità ed uniformità del “verde” presente all’interno dei tratti addominali dove è stata iniettata la sostanza e, come tale, percepita dal chirurgo. La valutazione di una vascolarizzazione residua sufficiente viene quindi tradizionalmente presa senza una quantificazione oggettiva della sua reale entità. A titolo di esempio, in Fig. 1 vengono mostrate due immagini di tratti addominali caratterizzati dalla presenza dell’ICG.
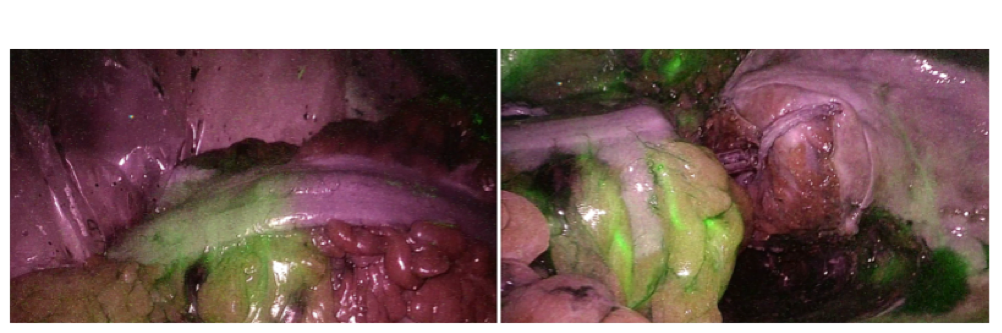
Figura 1: Applicazione di ICG in fase intraoperatoria prima e durante il confezionamento di una anastomosi intestinale: il verde indica il segmento intestinale perfuso e demarca il limite della sezione da effettuare.
Per questo motivo, il sistema proposto ricorre ad una valutazione automatica della luminosità e dell'uniformità del verde indocianina, impiegando una rete neurale che si serve di 20 “neuroni” per classificare i tratti di interesse come “ben vascolarizzati” oppure “scarsamente vascolarizzati”. Tale sistema fornisce quindi un risultato oggettivo ed è destinato ad essere un valido supporto decisionale per i chirurghi nella scelta della migliore strategia da adottare durante l’operazione.
Il funzionamento del sistema è sintetizzato in Fig. 2. Come visibile, l’input del sistema è lo streaming video proveniente in diretta dall’endoscopio. Inoltre, il chirurgo può scegliere, mediante l’ausilio di un PC, quale sia la regione di interesse (ROI) da ispezionare. Una volta stabilita la regione di interesse ed inizializzato il flusso dati con l’endoscopio, l’algoritmo sviluppato traccia la regione selezionata durante tutta l’esecuzione dello streaming video. Così facendo, è possibile delineare le caratteristiche (features) della ROI da fornire al classificatore, vale a dire la suddetta rete neurale. L’output fornito dal classificatore è infine corrispondente ad una “buona” od “insufficiente” vascolarizzazione.
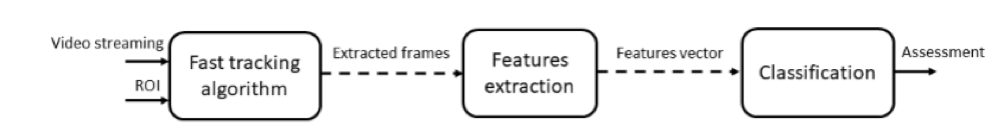
Figura 2: Architettura del sistema proposto
L'algoritmo è stato validato su un set di video catturati durante le procedure chirurgiche presso l'Ospedale Universitario Federico II di Napoli. I risultati ottenuti dal prototipo mostrano un'accuratezza media di classificazione pari al 99.9%.
Stato dell'attività
in fase to start up
Numero di pubblicazioni strettamente pertinenti, partecipazioni a convegni/ conferenze:
- Esposito C, Escolino M, Saxena A, Montupet P, Chiarenza F, De Agustin J, Draghici IM, Cerulo M, Sagaon MM, Di Benedetto V, Gamba P, Settimi A, Najmaldin A. European Society of Pediatric Endoscopic Surgeons (ESPES) guidelines for training program in pediatric minimally invasive surgery. Pediatr Surg Int. 2015;31(4):367-73. doi: 10.1007/s00383-015-3672-5.
2. Escolino M, Turrà F, Settimi A, Esposito C. Training for MIS in pediatric urology: proposition of a structured training curriculum. Transl Pediatr. 2016;5(4):315-323. doi: 10.21037/tp.2016.09.07.
3. Esposito C, Escolino M, Draghici I, Cerulo M, Farina A, De Pascale T, Cozzolino S, Settimi A. Training Models in Pediatric Minimally Invasive Surgery: Rabbit Model Versus Porcine Model: A Comparative Study. J Laparoendosc Adv Surg Tech A. 2016;26(1):79-84. doi: 10.1089/lap.2015.0229. - Esposito C, Masieri L, Castagnetti M, Crocetto F, Escolino M. Letter to the Editor: Robot-Assisted and Minimally Invasive Pediatric Surgery and Urology During the COVID-19 Pandemic: A Short Literature Review. J Laparoendosc Adv Surg Tech A. 2020;30(8):915-918. doi: 10.1089/lap.2020.0251.
- Cini C, Bortot G, Sforza S, Mantovani A, Landi L, Esposito C, Escolino M, Masieri L. Paediatric urology practice during COVID-19 pandemic. J Pediatr Urol. 2020;16(3):295-296. doi: 10.1016/j.jpurol.2020.04.023.
- Mamone V, Viglialoro RM, Cutolo F, Cavallo F, Guadagni S, Ferrari V. Robust laparoscopic instruments tracking using colored strips, in International Conference on Augmented Reality, Virtual Reality and Computer Graphics, 2017: Springer, pp. 129-143.
- Ferrari V, Ferrari M, Mosca F. Video see-through in the clinical practice, in EICS4Med, 2011, pp. 19-24.
- Gallo L. Hand shape classification using depth data for unconstrained 3D interaction. Journal of Ambient Intelligence and Smart Environments 2014;6(1): 93-105. doi:10.3233/AIS-130239.
- Gallo L. A study on the degrees of freedom in touchless interaction, SIGGRAPH Asia 2013, 19-22. doi:10.1145/2542355.2542390.
- Gallo L, Minutolo A. Design and comparative evaluation of Smoothed Pointing: A velocity-oriented remote pointing enhancement technique. International Journal of Human-Computer Studies 2012;70(4):287-300. doi:10.1016/j.ijhcs.2011.12.001.
- Gallo L, Placitelli AP, Ciampi M. Controller-free exploration of medical image data: Experiencing the Kinect. In 2011 24th international symposium on computer-based medical systems (CBMS) (pp. 1-6). IEEE
- Condino S, Turini G, Parchi PD, Viglialoro RM, Piolanti N, Gesi M, Ferrari M, Ferrari V. How to Build a Patient-Specific Hybrid Simulator for Orthopaedic Open Surgery: Benefits and Limits of Mixed-Reality Using the Microsoft HoloLens. J Health Eng. 2018;2018:5435097. doi: 10.1155/2018/5435097.
- Esposito C, Autorino G, Iervolino A, Vozzella E, Cerulo M, Esposito G, Coppola V, Carulli R, Cortese G, Gallo L, Escolino M. Efficacy of a virtual reality program in pediatric surgery to reduce anxiety and distress symptoms in the pre-operative phase. A prospective randomized clinical trial. J Laparoendoscopic Adv Surg Tech. 2021. IN PRESS.
Luogo ove viene svolta principalmente l'attività
UOC Chirurgia Pediatrica, UNINA